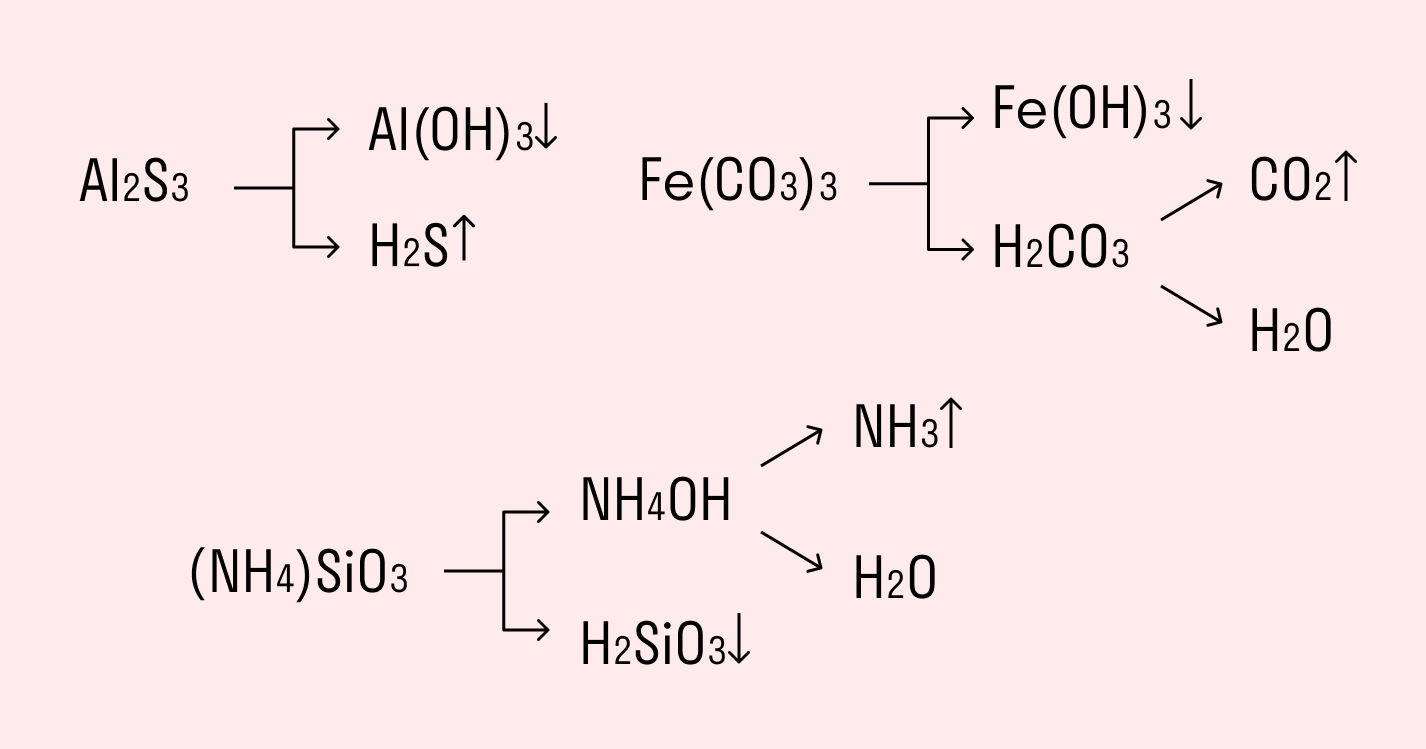
Отношение к гидролизу карбоната аммония

Как протекает гидролиз (NH4)2CO3?
Все курсы О курсе Азот Аммиак, соли аммония Получение и свойства аммиака Основные свойства аммиака Гидролиз солей аммония Гидролиз хлорида аммония Отношение солей аммония к нагреванию. Разложение нитратов Качественные реакции на нитрат-ион Окислительные свойства нитратов Порох. Азотистая кислота и нитрит Окислительно-восстановительные свойства нитритов Сравнение окислительно-восстановительной способности нитратов и нитритов.

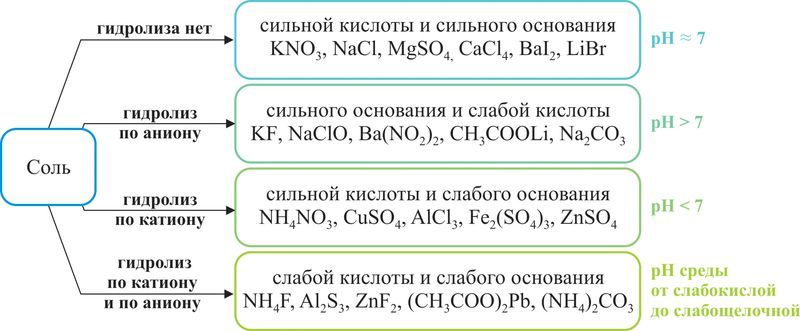

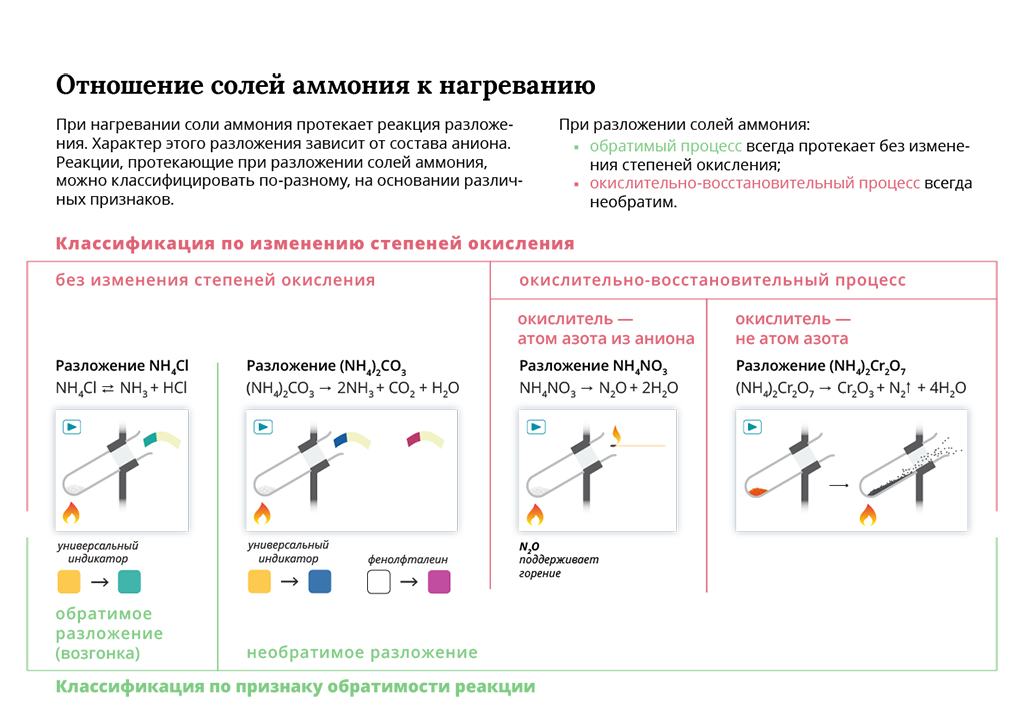




Гидролиз солей, образованных многозарядными катионами и анионами, протекает ступенчато, при этом в качестве промежуточных продуктов гидролиза образуются основные соли, если гидролиз идёт по катиону, и кислые соли, если гидролиз идёт по аниону. Каждая ступень гидролиза характеризуется своей константой. Для того, чтобы расcчитать константу гидролиза по заданной ступени, необходимо константу ионного произведения воды Kw разделить на константу диссоциации того слабого электролита, который образуется на данной ступени гидролиза. Пример 8. Диссоциация слабых электролитов протекает наиболее сильно по первой стадии и уменьшается с каждой последующей стадией:.

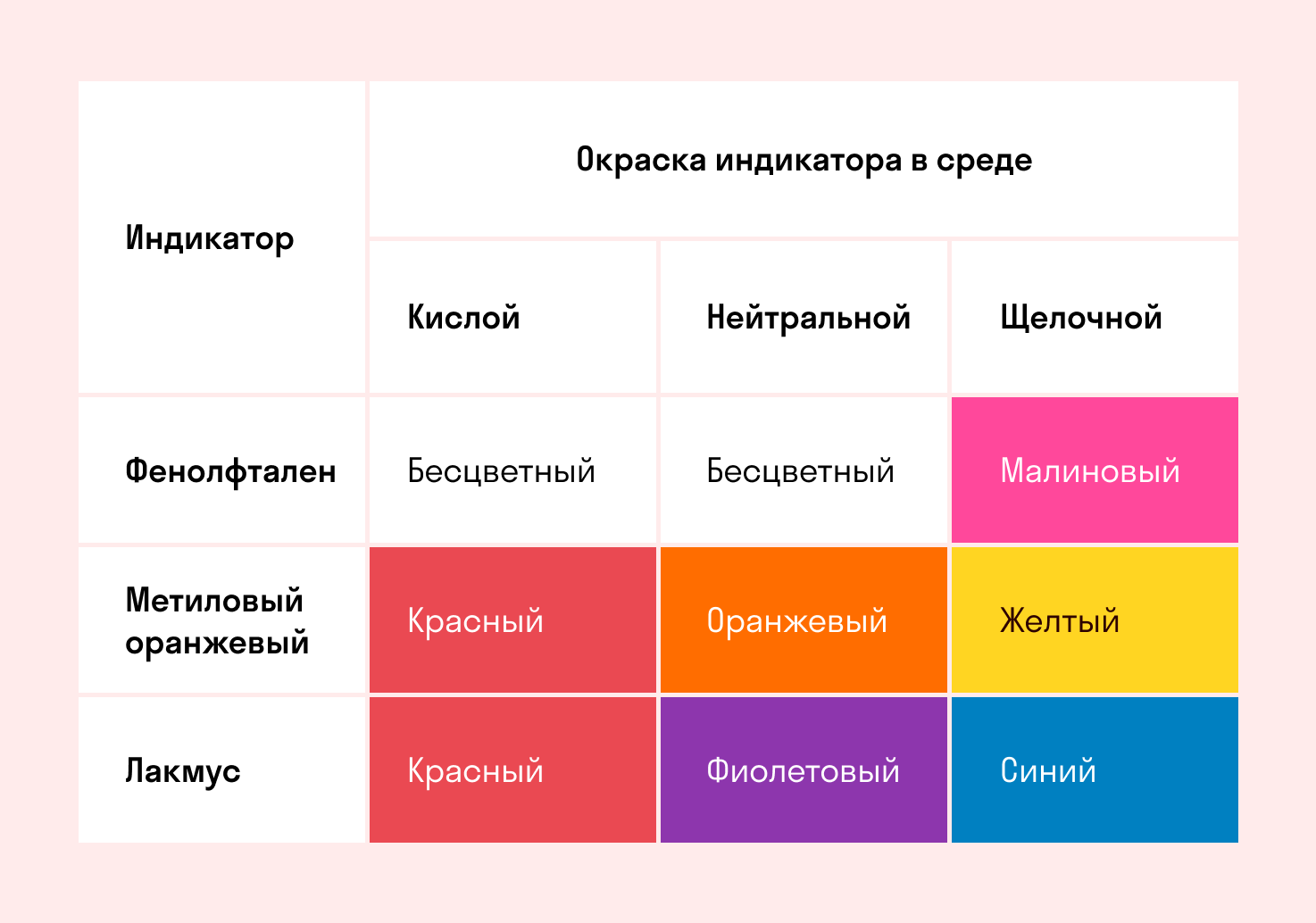


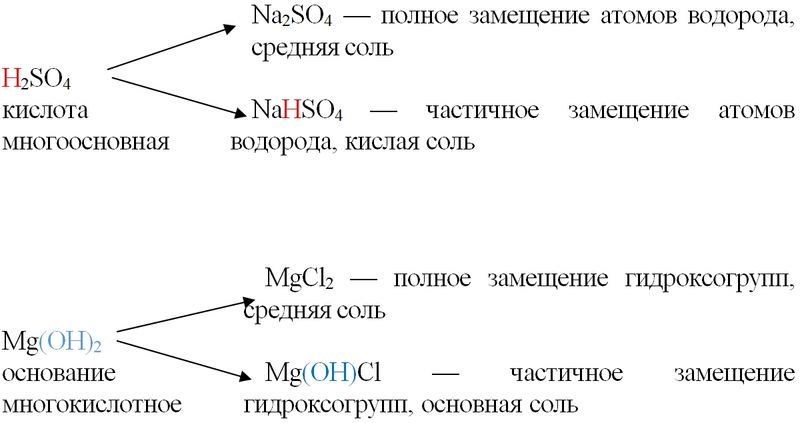




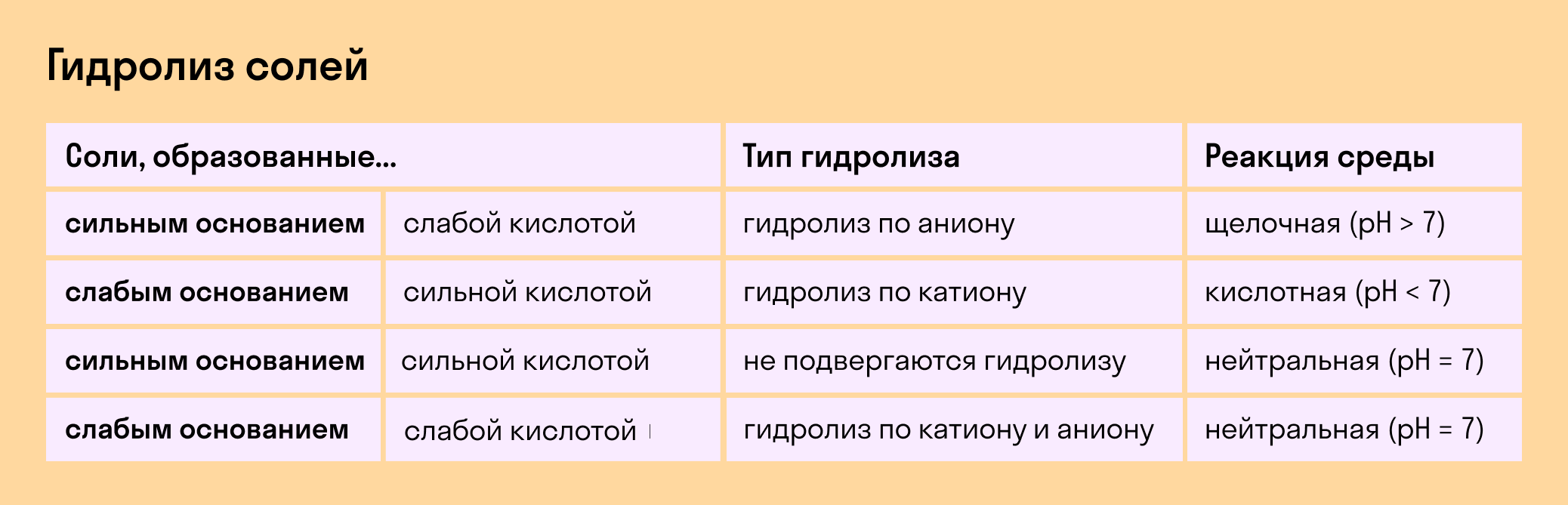

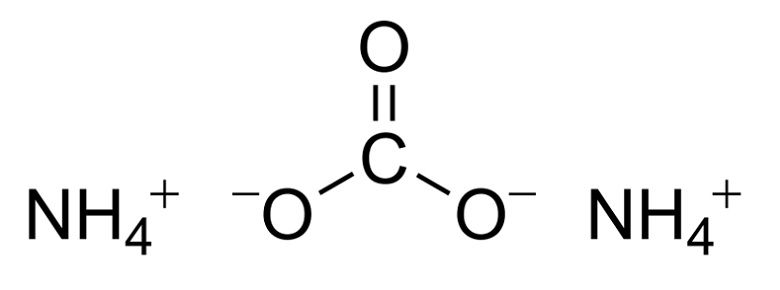

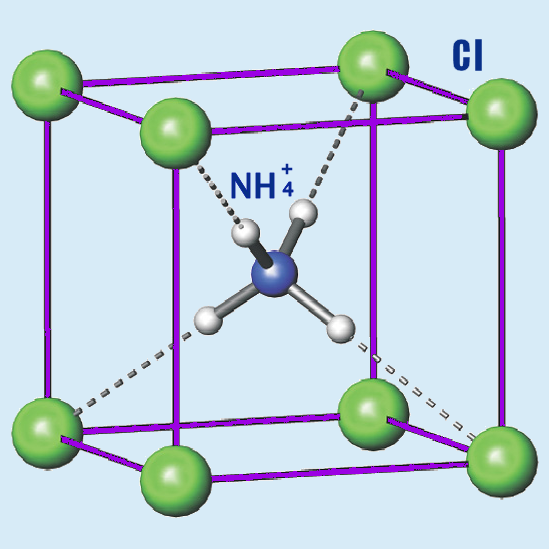
Карбонат аммония , углекислый аммоний, NH 4 2 CO 3 — аммониевая соль угольной кислоты. Бесцветные кристаллы. Хорошо растворим в воде. Очень неустойчив как на воздухе, так и в растворе, так как уже при комнатной температуре выделяет аммиак , превращаясь в гидрокарбонат аммония NH 4 HCO 3. На процессе разложения, связанном с выделением газов, основано применение карбоната аммония вместо дрожжей в хлебопечении и кондитерской промышленности пищевая добавка Е Карбонат аммония применяется для получения сульфата аммония из гипса по реакции.