Электронно графическая схема калия
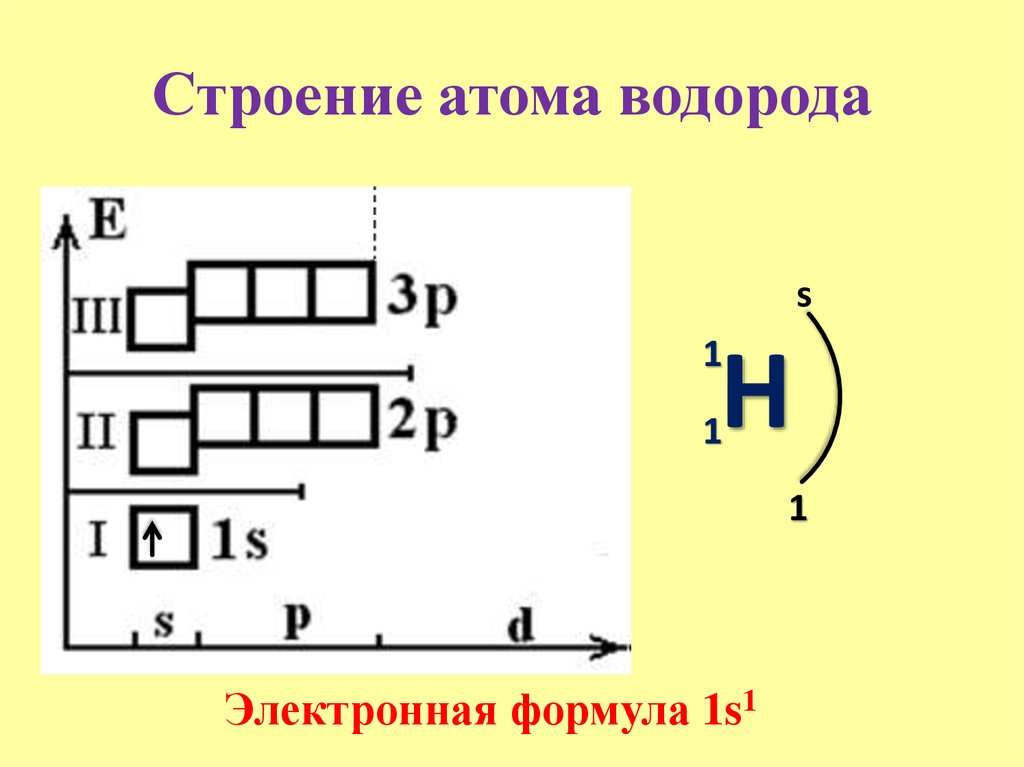
Электронная конфигурация атома калия (K)
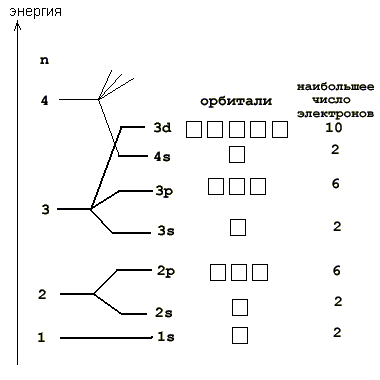
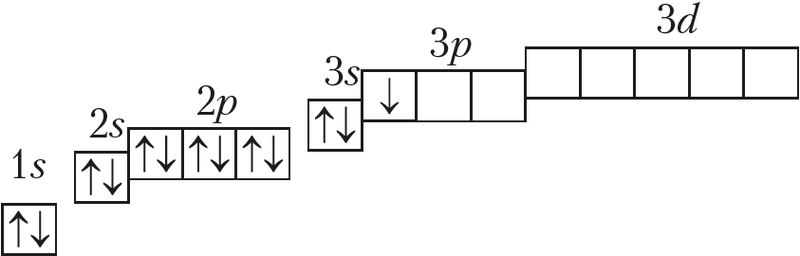
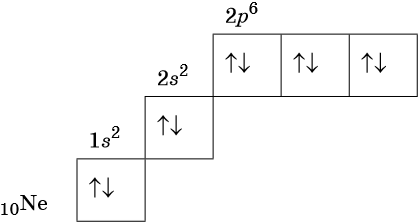
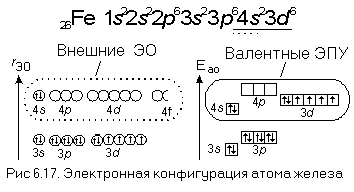
Начало см. Следовательно, для атома калия распределение электронов по орбиталям электронно-графическая формула имеет вид см. Калий относится к s -элементам со следующей электронной формулой конфигурацией атома:. Следовательно, скандий относится к d -элементам, и его атом характеризуется следующим распределением электронов по орбиталям:. Дополните рисунок так, чтобы показать вид одной s -орбитали и трех р -орбиталей, ориентированных вдоль осей. Последовательность заполнения энергетических уровней атомов см.




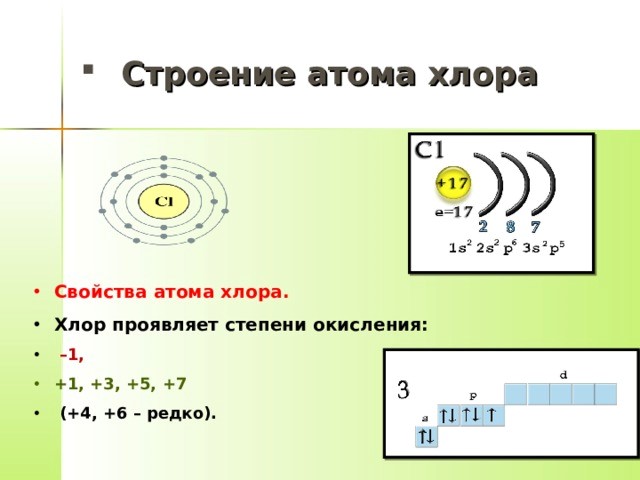
При нормальных условиях хлор является резко пахнущим газом, желто-зеленый цвет которого становится особенно заметным, когда в смеси с воздухом опускается вниз. Обусловлено это тем, что хлор тяжелее воздуха. К органолептическим свойствам также относится его «металлический» вкус. Среди основных химических свойств — высокая химическая активность, заключающаяся в способности образовывать соединения со многими элементами таблицы Менделеева. Объясняется высокая химическая активность особенностями молекулярного и атомного строения.



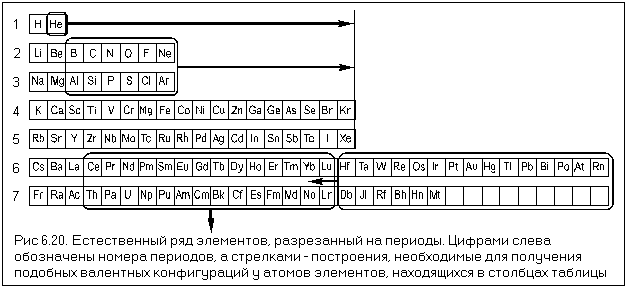
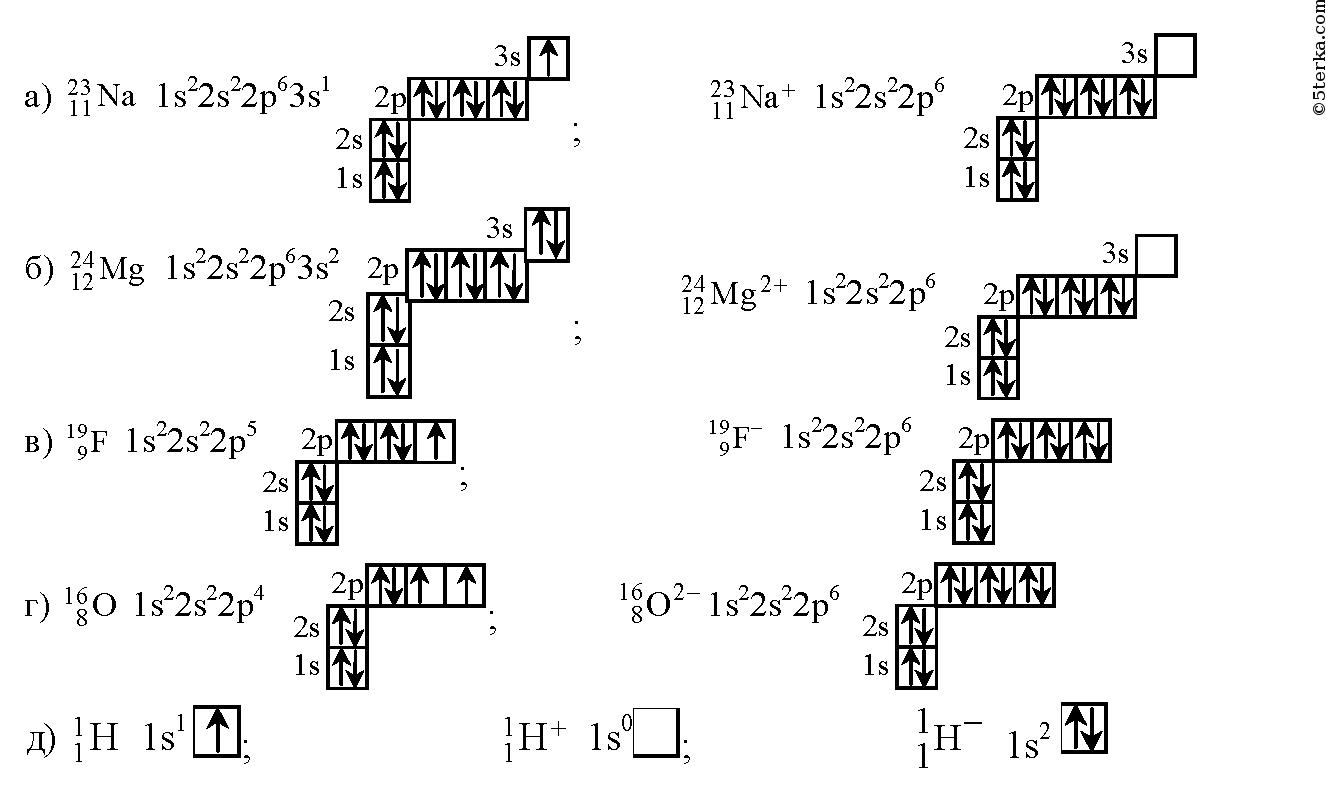


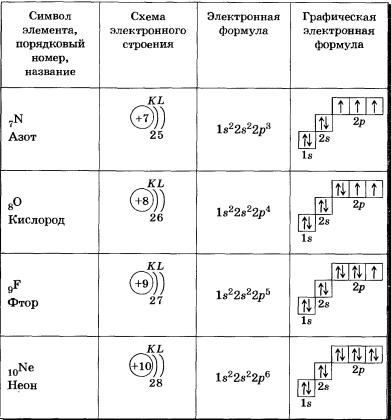

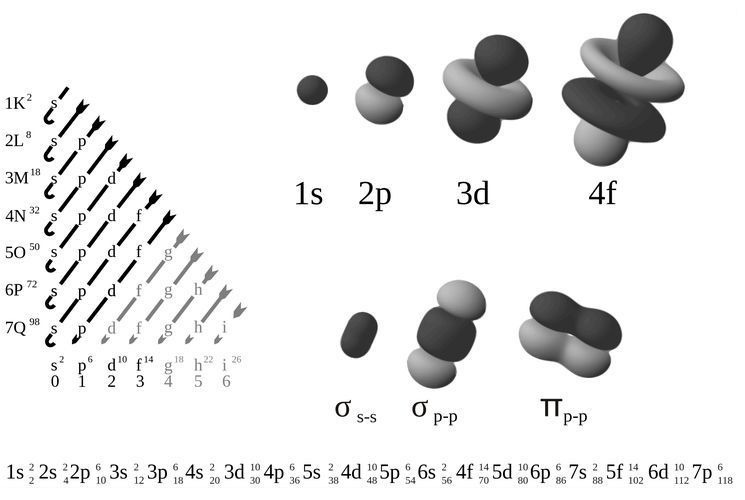
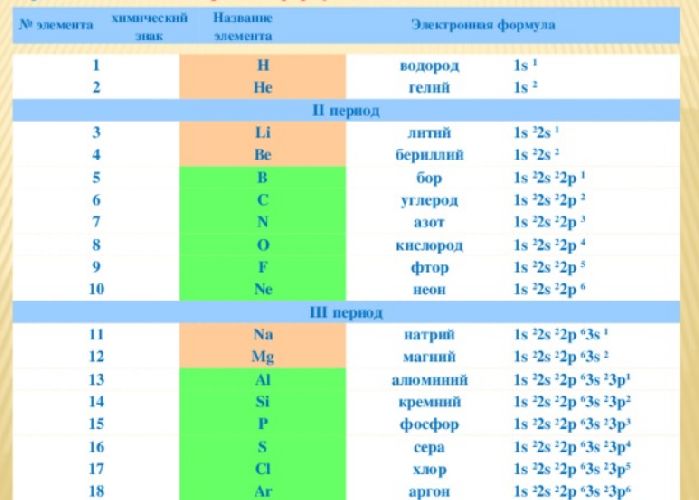
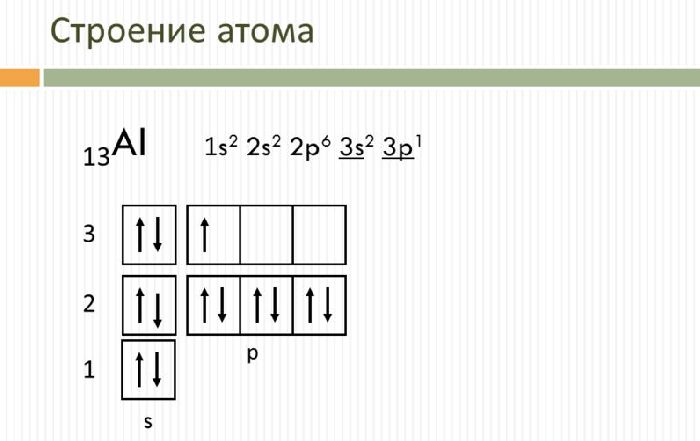
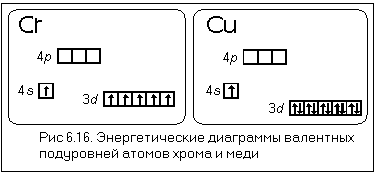
Электронные формулы атомов химических элементов, слои расположены в порядке заполнения подуровней. Электронные слои атомов заполняются электронами в порядке, согласно правилу Клечковского. Эмпирическое правило Клечковского и вытекающее из него схема очерёдностей несколько противоречат реальной энергетической последовательности атомных орбиталей только в двух однотипных случаях: у атомов Cr, Cu, Nb, Mo, Ru, Rh, Pd, Ag, Pt, Au имеет место «провал» электрона с s-подуровня внешнего слоя на d-подуровень предыдущего слоя, что приводит к энергетически более устойчивому состоянию атома, а именно: после заполнения двумя электронами орбитали 6s следующий электрон появляется на орбитали 5d, а не 4f, и только затем происходит заселение четырнадцатью электронами орбиталей 4f, затем продолжается и завершается заселение десятиэлектронного состояния 5d. Аналогичная ситуация характерна и для орбиталей 7s, 6d и 5f. Может ли кто-нибудь посоветовать наиболее удобную программу для создания электронных формул молекул в электронном виде? Войдите, чтобы оставить комментарий.